研究背景
趋化因子(chemokines)是一类具有趋化作用的细胞因子,最初认为趋化因子在炎症反应中调节白细胞定向移动而得名。但随后的研究发现趋化因子具有广泛的生物学作用。除参与炎症反应外,趋化因子及其受体在淋巴细胞归巢、免疫应答、感染、自身免疫性疾病、移植免疫排斥及血管生成等众多生理、病理过程中起着非常重要的作用。越来越多的证据表明趋化因子与肿瘤的生长、侵袭和转移密切相关。
趋化因子是细胞因子超家族成员中一大类具有化学趋化作用的分泌型小分子蛋白质(8-11kD)。自第一个趋化因子于80年代末被确认以来,迄今已发现至少50种趋化因子。趋化因子受体属于G蛋白偶联的7次跨膜受体超家族。不同类型的趋化因子通过与相应受体结合发挥作用。但部分趋化因子与受体结合特异性不强,即一种趋化因子可与多种受体结合,而一种趋化因子受体也可与多种趋化因子结合,不过亲和力有所不同。研究显示许多肿瘤细胞、肿瘤间质细胞和宿主细胞能自主分泌趋化因子及表达趋化因子受体。肿瘤相关趋化因子不仅可促进肿瘤细胞增殖、抑制其凋亡,而且还可以控制肿瘤细胞迁移、调节肿瘤血管生成、趋化淋巴细胞浸润肿瘤组织、参与肿瘤细胞器官选择性转移。如下图所示。
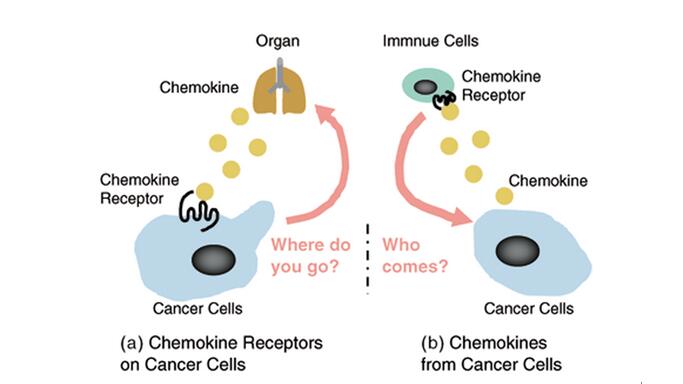
增殖是肿瘤侵袭转移的前提和基础。转移至靶器官的肿瘤细胞要形成转移灶也有赖于自身的增殖能力。肿瘤细胞分泌的某些趋化因子可以促进肿瘤细胞生长和(或)抑制其凋亡。恶性黑色素瘤细胞持续产生GRO-α和IL-8趋化因子,而其自身也同时高表达上述两种趋化因子的受体一CXCR2。GRO-α和IL-8通过自分泌方式直接刺激肿瘤细胞生长。此外IL-8也可通过自分泌方式促进肝癌、胰腺癌和结肠癌细胞增殖。Ruckes等报道成人T细胞白血病细胞高表达I-309及受体CCR8,I-309与CCR8结合可以抑制成人T细胞白血病细胞凋亡。肿瘤间质细胞、宿主细胞分泌的趋化因子亦可通过旁分泌机制发挥上述作用。
趋化因子与相应受体结合可引起细胞内肌动蛋白聚合,调节细胞运动和迁移。Kawada等在研究恶性黑色素瘤淋巴结转移时发现B16F10恶性黑色素瘤细胞持续表达CXCR3趋化因子受体,受配体CXCL9、CXCL10及CXCL11等趋化因子刺激后,细胞内F-肌动蛋白水平升高,并发生聚合,细胞骨架蛋白重排。肿瘤细胞朝趋化因子浓度梯度方向移动,突破纤维连接蛋白覆盖的聚碳酸酯滤膜能力明显增加,并呈剂量、时间依赖性。Muller等报道SDF-1趋化因子可以使乳腺癌细胞做定向运动,穿透人工重建基底膜。而抗CXCR4抗体能阻断该作用。
肿瘤的转移并非随机过程,不同类型的肿瘤有各自的器官转移倾向性。对于这种器官选择性转移有不同的解释。“种子与土壤”学说认为,转移的肿瘤细胞随机分布于全身,但只有在提供适宜生长环境的组织或器官中才得以生存、增殖。第2种解释认为靶器官的血管内皮细胞表达特异性粘附分子,可以捕获循环中肿瘤细胞。第3种理论认为靶器官具有特异性趋化因子,吸引特定肿瘤细胞归巢。以往这种理论用于解释造血干细胞特异性归巢于骨髓,而最近Muller等证实趋化因子及其受体在决定肿瘤转移部位上也起着非常重要的作用。乳腺癌原发此及转移灶组织中趋化因子受体CXCR4和CCR7表达显著高于正常乳腺组织,而乳腺癌常见转移部位(淋巴结、肺、肝脏和骨髓)中这两种受体的配体SDF-1α和6Ckine趋化因子表达水平远髙于罕见转移邰位(小肠、皮肤、脑组织和骨骼肌)的表达水平。体外试验进一步证实SDF-1α和6Ckine可诱导乳腺癌细胞做趋化运动,穿透人工重建基底膜,并呈剂量依赖性方式。而抗CXCR4或抗6Ckine的抗体能阻断这种作用。正常肺、肝脏组织的提取物对乳腺癌细胞有明显的趋化作用,但皮肤、肌肉这些乳腺癌罕见转移部位的组织提取物趋化作用不显著。体内实验发现,抗CXCR4单抗能有效地抑制原位种植于严重联合免疫缺陷小鼠的人乳腺癌细胞自发性肺转移和淋巴结转移。恶性黑色素瘤除了与乳腺癌有相似的转移部位外,还易转移至皮肤。Muller等发现,恶性黑色素瘤细胞系除高表达CXCR4和CCR7外,还表达高水平的CCR10,而CCR10配体CTACK正是皮肤所含的特异性趋化因子。
研究模型
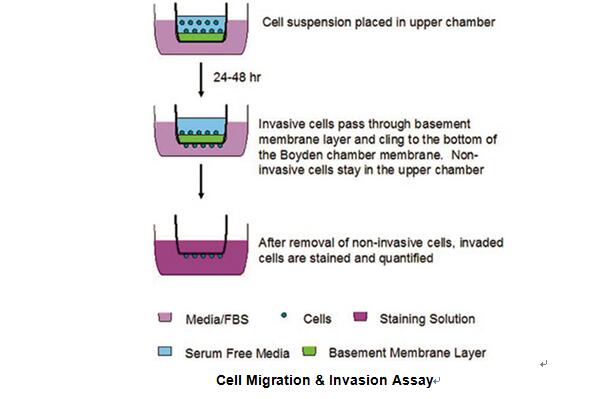
我们建立了肿瘤转移的研究模型,包括体外(浸润模型)和体内(转移模型)。体外模型主要研究:1)肿瘤细胞对结蹄组织上皮细胞基质分子的降解,包括laminin、fibronectin、collagen等;2)肿瘤细胞对一些生物膜的穿透力;3)新血管的形成能力;4)体外肿瘤细胞的聚集性和运动性。体内模型主要研究肿瘤细胞的转移性,即肿瘤细胞在远端组织形成病灶的能力。在选择药物作用研究时,可以通过两种方法:1)将准备注射的肿瘤细胞先用药物在体外培养并发生作用,然后将药物作用后的瘤细胞接种于小鼠血管;2)将药物直接注射入受体小鼠,再对小鼠血管内注射肿瘤细胞。如下图所示。
Copyright © 2008 - 2018 上海诺百生物科技有限公司 版权所有
技术咨询信箱:techsupport@novobiosci.com 订单查询信箱:sales@novobiosci.com
地 址:上海市闵行区顾戴路3100弄789号2楼 苏ICP备12010280号